Hoe een advocatenkantoor in naam van de patiënt tegen lagere medicijnprijzen lobbyt

Advocatenkantoor KienLegal voerde de afgelopen jaren de belangrijkste taken uit voor een aantal patiëntenstichtingen, maar hielp daarmee ook opvallend vaak farmaceutische of medische voedingsbedrijven. Een eerste blik in een juridische trukendoos waarin een ontelbaar aantal petten lijkt te zitten.
Dit is het bedrijfsadres op de K.P. van der Mandelelaan 74, te Rotterdam. Schrik niet van de rechtspersonen en hoe ze met elkaar in verband staan:
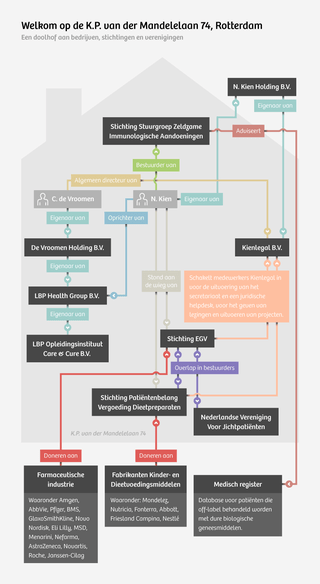
Je ziet, een wirwar aan stichtingen, bv’s en zelfs een patiëntenvereniging.
De Stichting Eerlijke Geneesmiddelenvoorziening is de bekendste instantie op dit adres, de stichting met de illustere naam Patiëntenbelang Ondervoeding en Vergoeding Dieetpreparaten (SPVD) is vooral bekend van rechtbankverslagen.
Rechtbankverslagen?
Ja, want wat deze instanties met elkaar gemeen hebben, is dat ze niet alleen een kantoor delen, maar ook van de diensten van het advocatenkantoor KienLegal gebruikmaken, een gespecialiseerd bureau op het gebied van farmaceutisch recht.
Hoe verhouden al deze stichtingen zich tot dit advocatenkantoor? Naar de buitenwereld worden ze slechts ‘samenwerkingspartners’ genoemd. ‘Cliënten,’ noemt praktijkeigenaar Nicole Kien ze, die ‘geen enkele organisatorische of bestuurlijke vermenging’ hebben met haar bedrijfsvoering. Dat verzekert de jurist in een lange reactie op dit artikel.
De bestuurders van deze stichtingen doen hun werk niettemin veelal kosteloos en wenden vrijwel al het geld van de stichtingen aan om KienLegal in te huren voor ‘het uitvoeren van projecten,’ ‘een juridische helpdesk,’ ‘het geven van lezingen’ of ‘de uitvoering van het secretariaat,’ En dus: het voeren van rechtszaken.
Wat voor rechtszaken? Kien vertelde vrijdag 11 december in Nieuwsuur dat haar advocatenteam ‘al regelmatig aan de rechtbank heeft moeten vragen om de zorgverzekeraar te verplichten tot nakomen van de zorgplicht,’ vaak in gevallen waar een patiënt ‘binnen het ziekenhuis geen toegang kreeg tot een duur geneesmiddel dat wel noodzakelijk was.’
In veel van die procedures tegen zorgverzekeraars vertegenwoordigt het kantoor een patiëntenvereniging, of pikanter: een van de patiëntenstichtingen waaraan Kien naar eigen zeggen aan de wieg stond en die gevestigd zijn op hetzelfde adres als haar advocatenpraktijk. Zoals de SPVD.
De producenten van de betwiste geneesmiddelen of medische voedingsproducten schenken bij elkaar jaarlijks tonnen aan deze stichtingen. Tussen 2008 en 2014 ontving alleen al de Stichting Eerlijke Geneesmiddelenvoorziening bijna een miljoen euro van farmaceutische bedrijven.
Het roept de vraag op of het hier wel exclusief om de patiënt gaat.
Met die firma’s onderhoudt de zorgjurist, buiten haar werkzaamheden voor de stichtingen, een nauwe band. Kien geeft persoonlijk geaccrediteerde nascholingscursussen aan artsen en medisch specialisten. Namens farmaceutische bedrijven als Roche bijvoorbeeld, de grootste producent van kankermedicijnen.
Ook zit Kien in het bestuur van de Stichting Stuurgroep Zeldzame Immunologische Aandoeningen, een mondvol waarvan nauwelijks iets bekend is anders dan dat de stichting een medisch register adviseert waarin patiënten worden bijgehouden die worden behandeld met dure middelen van fabrikanten die geen vergunning hebben voor de desbetreffende ziekte.
Hoe zit dat? Farmaceutische bedrijven mogen onder geen enkel beding geneesmiddelen aanbevelen voor aandoeningen waarvan niet is aangetoond dat ze effectief en veilig zijn; artsen mogen onder strikte voorwaarden wel medicijnen voorschrijven die niet bewezen veilig zijn. De vraag is: waarom zit een advocaat die alles weet van vergoeding, ook bij patiënten die off-label worden behandeld, en heel korte lijntjes heeft met de bedrijfstak, in het bestuur van een stichting die een dergelijk register adviseert?
Ze is ook te gast op opleidingsbijeenkomsten van ‘samenwerkingspartner’ en nascholingsbureau LBP Health Group. Een onderneming in het bezit van Cornelis de Vroomen, die weer de algemeen directeur is van KienLegal. Daar spreekt de jurist dan namens de Stichting Eerlijke Geneesmiddelenvoorziening, zoals ze bij een bijeenkomst in oktober te kennen gaf. Een die - volgen jullie het nog? - ook nog in samenwerking met lobbyorganisatie Nefarma werd georganiseerd.
Kortom: het is lastig te volgen welke rol de jurist op welk moment speelt.
Wordt de patiënt nog verdedigd?
Het komt overeen met wat talloze betrokkenen de afgelopen jaren met de Stichting Eerlijke Geneesmiddelenvoorziening, de bekendste partij op het adres, hebben zien gebeuren.
Nu de bestuurders van de stichting te oud worden of met gezondheidsproblemen kampen, worden er meer en meer taken overgedragen aan het advocatenkantoor, dat ook farmaceuten als cliënten heeft.
Van het exclusief verdedigen van patiëntenbelangen lijkt steeds minder sprake
Zonder uitzondering spreken zowel belanghebbenden als onafhankelijke bronnen lovend over wat de stichting en diens juristen voor de patiënt in het verleden hebben gedaan. Maar van het exclusief verdedigen van patiëntenbelangen lijkt steeds minder sprake.
Bijvoorbeeld door aanhoudend twijfels te zaaien over goedkopere vervangers van middelen die geen octrooibescherming meer genieten. Zelfs als de registratieautoriteit geen reden meer ziet voor die twijfels. Of in sommige procedures tegen zorgverzekeraars, die door KienLegal worden gevoerd.
Een zaak omgeven met belangen
Een voorbeeld. Eind 2014 start Achmea met een inkoopexperiment. De zorgverzekeraar wil met een aantal ziekenhuizen dure medicijnen gaan inkopen, om zo kortingen te bedingen bij farmaceutische bedrijven.
Hoe gaat dat in zijn werk? Dat is een beetje een technisch verhaal, maar komt op het volgende neer.
Achmea laat ziekenhuizen een contract tekenen. Daarin beloven de ziekenhuizen om circa 80 procent van de nieuwe patiënten op het voordeligste aangewezen middel te zetten.
Ziekenhuizen kunnen er nog steeds voor kiezen om niet mee te doen en zelf te blijven onderhandelen, maar dan krijgen ze maar 80 procent van de vastgestelde vergoedingsprijs voor de desbetreffende medicijnen van Achmea terug.
Per ziektebeeld mogen fabrikanten met vergelijkbare middelen bij Achmea een bod uitbrengen; degene die het laagst biedt, mag het zogenoemde voorkeursmiddel leveren.

Het experiment komt de verzekeraar op een rechtszaak te staan. Janssen-Cilag, een dochterbedrijf van farmareus Johnson & Johnson en aanbieder van een zogenoemde interleukineremmer, acht de inkoopprocedure in strijd met de wet.
Niet eens zozeer omdat het bedrijf er zelf door wordt geraakt, blijkt uit de pleitnota. Nee, het belangrijkste argument van het bedrijf is dat ‘de aanspraak’ van patiënten en de ‘onafhankelijke beroepsbeoefening’ van medisch specialisten door Achmea worden ingeperkt.
Met andere woorden: het bedrijf begint een procedure omdat de verzekeraar op de stoel van de arts gaat zitten. De specialist en daardoor de patiënt zouden er de dupe van zijn.
En hoewel de beroepsgroep geen partij is in de rechtszaak - ‘blijkbaar is er niet zo zwaar aan getild,’ aldus de woordvoerder - voegt de relatief kleine, door vrijwilligers gerunde patiëntenvereniging Psoriasis Vereniging Nederland zich later in de procedure tegen de zorgverzekeraar. Ook zij blijken zich ineens gedupeerd te voelen.
KienLegal vertegenwoordigt de vereniging in deze zaak.
De klagers krijgen bijval uit academische hoek, van universitair docent farmaceutisch recht Marie-Hélène Schutjens. Ze is tegen, ‘omdat dit mogelijk de behandelopties en dus de rechten van verzekerden beperkt,’ zo tekent een vakblad uit haar mond op. ‘Het gaat immers niet om identieke producten, dus verschraling dreigt.’
Professor Schutjens is getrouwd met de general manager van Janssen-Cilag Nederland, Paul Korte. Ze was ook jarenlang de jurist van koepelvereniging Nefarma.
De zaak is op allerlei vlakken omgeven met bedrijfsmatige belangen. Is het echt de patiënt die centraal staat in deze klacht?
De argumenten van de advocaat van KienLegal, die handelt namens de patiëntenvereniging, lijken één op één ontleend aan die van Janssen-Cilag. Ook die zijn sterk opgebouwd met informatie van direct belanghebbende partijen: de firma’s Pfizer, AbbVie en Janssen-Cilag, die omzet dreigen te verliezen.
De advocaat van KienLegal haalt een enquête-onderzoek aan. Medisch specialisten zouden overwegend negatief zijn over, of onbekend zijn met de inkoopactie van Achmea, is de conclusie. Slecht idee dus om met deze actie door te gaan.
De advocaten van Janssen-Cilag verwijzen eveneens naar het onderzoek, dat in opdracht van AbbVie, een directe concurrent van Janssen-Cilag, is gemaakt.
Het bedrijf heeft wel meegeboden bij Achmea en heeft een voorkeurspositie gewonnen voor dermatologische aandoeningen. Waarom heeft een concurrent die deze inkoopactie voor de rechter ongedaan wil krijgen een dergelijk document van AbbVie? Wordt er achter de schermen gelobbyd om de grootschalige inkoop aan diggelen te procederen?
Het mag allemaal niet baten. De rechter verwerpt alle aantijgingen en merkt fijntjes op dat ‘hoewel Janssen-Cilag vooral een beroep doet’ op de bescherming van patiëntbelangen, de claims vooral heeft ‘gebaseerd op onrechtmatig handelen door Achmea jegens haar.’
Met andere woorden: patiënt noch specialist is hier de dupe, volgens de rechter.
Hoe laat je alternatieve middelen onveilig lijken?
In de complexe discussie over de nieuwste generatie goedkopere kopiemedicijnen, biosimilars, speelt de Stichting Eerlijke Geneesmiddelenvoorziening de producenten van dure merkgeneesmiddelen zelfs in de kaart.
Een korte samenvatting: de discussie over biosimilars is de laatste maanden in een stroomversnelling geraakt. De bekendste drie TNF-alfa-remmers, een jaarlijkse kostenpost van meer dan 500 miljoen euro, lopen sinds 2014 in rap tempo uit patent.
Dat zorgt ervoor dat andere fabrikanten veel goedkopere afgeleiden - biosimilars - op de markt brengen, waardoor de komende jaren naar schatting 200 miljoen euro per jaar bespaard kan worden. Het is voor het eerst dat blockbusters van dit kaliber in aanmerking komen voor kopieproductie.
Veel geld, dat hard nodig is om heel dure middelen, bijvoorbeeld de nieuwste kankermedicijnen, een plaatsje in het ziekenhuisbudget te geven.
Maar de bedrijven die de originele producten - specialités - verkopen, zien heel veel omzet verdampen. En hebben er dus alle belang bij dat er onzekerheid over de veiligheid van deze alternatieven bestaat.
Zo werpt de industrie de vraag op of bestaande patiënten die met het merkproduct worden behandeld, veilig overgezet kunnen worden op de biosimilar.
En daar speelt de Stichting Eerlijke Geneesmiddelenvoorziening, bij monde van diens juristen, een curieuze rol in.
Een onvindbaar positioneringsdocument
Ook hier duikt ineens een stichting op die de agenda van fabrikanten kracht bijzet met patiëntengrieven. De Nederlandse Hypofyse Stichting, een kleine patiëntenclub, stuurt in december 2014 een persbericht de wereld in waarin wordt gewaarschuwd voor het omzetten van patiënten naar een biosimilar.
Patiënten ‘worden de dupe’ van de strijd over de kosten die verzekeraars, ziekenhuizen en farmaceuten over geneesmiddelen voeren, stelt de stichting. Van omzetten naar een biosimilar is nog veel te weinig bekend, waardoor patiënten worden blootgesteld aan ‘onaanvaardbare risico’s.’
Het is juist tegen het belang van patiënten om dure middelen te blijven voorschrijven
De bezorgde patiënten baseren zich voor een groot deel op een zogenoemd ‘position paper’ over biosimilars van de Stichting Eerlijke Geneesmiddelvoorziening. Een document dat tot op de dag van vandaag niet ter inzage beschikbaar is.
De vraag is: zijn de patiënten terecht bezorgd?
Twee hoogleraren gespecialiseerd in biologische geneesmiddelen vinden van niet. De waarschuwing van de stichting kan ‘de toets der wetenschappelijke kritiek’ niet doorstaan, stellen Arnold Vulto van het Erasmus MC en Huub Schellekens van de Universiteit Utrecht. Ze klimmen in de pen voor een reactie op de oproep van de Hypofyse Stichting, omdat zij van mening zijn dat patiënten zonder goede reden ongerust worden gemaakt.
Zij sturen een puntsgewijze ontkrachting van negen pagina’s met verwijzingen naar wetenschappelijke publicaties rond, waarin ze concluderen dat het bericht van de Hypofyse Stichting ‘onnodig onrust zaait.’

Patiënten kunnen door de medisch specialist probleemloos worden overgezet op een biosimilar, stellen zij. Er zijn namelijk genoeg langetermijngegevens beschikbaar. Nog belangrijker: in een tijd waarin ‘de betaalbaarheid van de gezondsheidzorg in Nederland onder druk staat’ denkt ‘ieder weldenkend mens’ na over hoe besparingen kunnen worden geboekt bij ‘gelijkblijvende kwaliteit,’ aldus de professoren. Ook op het gebied van medicijnen.
Met andere woorden: het is juist tegen het belang van patiënten om dure middelen te blijven voorschrijven als er goedkopere kopieproducten beschikbaar zijn.
Het commentaar komt de kleine patiëntenclub op een berg kritiek te staan, maar de Stichting Eerlijke Geneesmiddelenvoorziening, de partij die de Hypofyse Stichting via de achterdeur ongerust gemaakt heeft, blijft buiten schot.
Waarom stuurt die stichting informatie over biosimilars rond die niet in het openbaar in te zien is? En nog opvallender: waarom neemt ze geen verantwoordelijkheid als een kleine patiëntorganisatie onder vuur genomen wordt voor uitingen die uit haar eigen koker komen?
Mede mogelijk gemaakt door AbbVie
Uit presentaties van lezingen die Nicole Kien en een advocaat van KienLegal in het land gaven, blijkt wat de strekking van het ‘position statement’ over biosimilars van Eerlijke Geneesmiddelenvoorziening is.
De stichting ontving 10.000 euro van AbbVie, de farmaceut achter tnf-alfa-remmer Humira die in 2018 in Europa voor biosimilarconcurrentie in aanmerking komt. Er is geen bedrijf ter wereld dat zo wordt bedreigd door biosimilars als AbbVie.
Het belangrijkste uitgangspunt van het ‘position paper’ van Eerlijke Geneesmiddelenvoorziening: de portemonnee mag nooit een reden zijn om patiënten over te zetten op een biosimilar. ‘Niet-medisch switchen,’ noemen juristen dat. En als dat standpunt niet wordt nagekomen, ‘is dat reden voor actie,’ belooft een advocaat in een presentatie.
Diametraal tegenover de verklaring van Vulto en Schellekens, die juist concluderen dat financiële overwegingen het enige bestaansrecht van de biosimilar zijn. Anders verlagen spécialitéproducenten hun prijzen immers nooit.
De Stichting Eerlijke Geneesmiddelenvoorziening is echter lang in goed gezelschap geweest in het voorzichtige standpunt over biosimilars: de registratieautoriteit en tevens de hoogste geneesmiddelautoriteit in Nederland, het College ter Beoordeling van Geneesmiddelen (CBG), heeft al sinds 2010 het standpunt dat ‘patiënten zo veel mogelijk op een biologisch geneesmiddel gehouden moeten worden als ze daar klinisch goed op reageren.’
Met andere woorden: switchen naar een biosimilar omdat het goedkoper is? Liever niet.
Registratieautoriteit: switchen kan
Maar het CBG is intussen op zijn stellingname teruggekomen. Na ‘zorgvuldige bestudering van de meest recente literatuur en ervaringen met de beoordelingen van biosimilars’ blijkt dat zijn strikte terughoudendheid niet meer van deze tijd is.
Switchen kan prima, maar het is de arts die hierover gaat, niet alleen de ziekenhuisapotheker en al helemaal niet de zorgverzekeraar
Switchen kan prima, concludeert de registratieautoriteit, maar het is de arts die hierover gaat, niet alleen de ziekenhuisapotheker en al helemaal niet de zorgverzekeraar.
Het komt de registratieautoriteit op een bezoek van Nicole Kien te staan, namens de Stichting Eerlijke Geneesmiddelenvoorziening. Ze is niet blij met met het nieuwe wetenschappelijke standpunt van de registratieautoriteit.
Dat gesprek leidt klaarblijkelijk niet tot het gewenste effect. Niet lang daarna wordt zelfs een spreekbeurt gegeven waarin wordt gesuggereerd dat een standpunt over biosmilars wettelijk gezien helemaal niet onder het takenpakket van de registratieautoriteit valt. En dus niet veel waarde heeft.
Opmerkelijk, want naar het oude CBG-standpunt is door de juristen van KienLegal altijd verwezen om te onderbouwen waarom overstappen op een biosimilar om ‘niet-medische redenen’ onverstandig is. Nu het CBG het tijd acht voor een herziening, stapt de registratieautoriteit klaarblijkelijk buiten haar wettelijke functie.
Is traceerbaarheid wel een probleem?
De Stichting Eerlijke Geneesmiddelenvoorziening, maar ook nascholingsbedrijf LBP Health Group, hebben de afgelopen maanden opnieuw gewaarschuwd voor het omzetten van patiënten op een biosimilar. Ook is een waarschuwingsbrief naar ziekenhuisdirecteuren gestuurd. Gek genoeg wordt hierbij alsnog het nieuwe standpunt van het CBG gebruikt.
Hoe? De stichting gooit het over een andere boeg: switchen naar biosimilars wordt niet langer als onzeker en dus onveilig bestempeld, maar - zo stelt de stichting nu - traceerbaarheid van biosimilars zou in Nederland niet goed geborgd zijn. Sterker, die zou zo slecht zijn dat Nederlandse ziekenhuizen in strijd handelen met Europese richtlijnen.

Opnieuw een bureaucratische horde, dit keer op het gebied van de geneesmiddelenbewaking.
Zolang de middelen per patiënt niet tot biosimilarbedrijf kunnen worden herleid, vindt de stichting het onverantwoord om patiënten over te zetten. Want, zo zegt het CBG, switchen moet gepaard gaan met ‘adequate klinische monitoring.’
Feit is dat in Nederland al meer dan vijftien jaar biologische geneesmiddelen worden voorgeschreven. Die allemaal al meerdere lichtingen gehad hebben, of zelfs tientallen productieaanpassingen hebben ondergaan.
Tussen al die merkmiddelen, zeker wat betreft de TNF-alfa-remmers, is maar wat vaak gewisseld. En toen waarschuwde nooit iemand voor gebrekkige registratie. In dit geval was dat nog urgenter geweest: het gaat immers om volstrekt andere moleculen.
Het CBG raadt artsen voor alle biologische geneesmiddelen aan, spécialité dan wel biosimilar, lichtingnummer en product in het patiëntdossier vast te leggen.
Gebeurt dat? Ja, maar in de meeste ziekenhuizen is een lichtingnummer niet direct met een muisklik terug te halen. Dat vergt enige inspanning. Moet dat beter? Daar is iedereen het over eens, maar dat wordt door niemand als serieuze reden gezien om geen biologische geneesmiddelen meer voor te schrijven.
Toch suggereert Eerlijke Geneesmiddelenvoorziening dat dit probleem specifiek op biosimilars van toepassing is, waardoor patiënten op de oude middelen moeten blijven staan.
Een stap te ver
De stichting trok het bericht terug waarin gesteld wordt dat Nederlandse ziekenhuizen de Europese richtlijnen aan hun laars lappen. Dat kwam neer op een rectificatie.
Die richtlijnen slaan namelijk op vervalste, gevaarlijke geneesmiddelen of op voorschriften over geneesmiddelenbewaking die nog niet eens zijn ingevoerd. Met andere woorden: Nederland is helemaal geen buitenbeentje in de Europese Unie op het gebied van de traceerbaarheid van biologische geneesmiddelen.
Tijdens de afronding van dit onderzoek werd bekend dat de stichting Eerlijke Geneesmiddelenvoorziening na tien jaar per 1 januari 2016 wordt opgeheven. Naar eigen zeggen door een gebrek aan geld. ‘Er bestaat niet langer voldoende financieel draagvlak voor deze vorm van onafhankelijke belangenbehartiging voor alle patiënten in Nederland,’ aldus Eerlijke Geneesmiddelenvoorziening in een verklaring. In een reactie laat Kien weten dat ook de Nederlandse Vereniging voor Jichtpatiënten wordt opgeheven.
Of zoals een bestuurder van de stichting in een reactie stelt: ‘Twee structurele subsidieverzoeken aan het ministerie van VWS hebben niet geleid tot structurele toegang tot niet aan de farmaceutische industrie gerelateerde financiering, hoewel de stichting daar graag toegang toe had gekregen.’
Eerlijke Geneesmiddelenvoorziening is wel met ‘diverse stakeholders’ in overleg of en waar het ‘gedachtegoed van de stichting Eerlijke Geneesmiddelenvoorziening het meest effectief kan worden ondergebracht.’
Zolang de politiek moeilijke beslissingen op het gebied van dure geneesmiddelen uitbesteedt aan de strijd van marktpartijen – zorgverzekeraars, ziekenhuizen en farmaceuten – is het een kwestie van tijd voordat van een partij die voor de patiëntenbelangen zegt op te komen, op een zeker moment ook niet meer helder is wiens agenda nu het belangrijkste is.

